原文:https://yjj.beijing.gov.cn/yjj/ztzl48/ylqxjgfwzn/jsscgfzl64/yycp60/11001531/index.html
发布时间:2021年06月02日
版权归属原文本规范旨在指导和规范X射线诊断设备的技术审评工作,帮助审查人员增进对该类产品机理、结构、主要性能、预期用途等方面的理解,方便审查人员在产品注册技术审评时把握基本的要求和尺度。
本规范所确定的核心内容是在目前的科技认识水平和现有产品技术基础上形成的,因此,审评人员应注意其适宜性,密切关注适用标准及相关技术的最新进展,考虑产品的更新和变化。
本规范不作为法规强制执行,不包括行政审批要求。但是,审评人员需密切关注相关法规的变化,以确认申报产品是否符合法规要求。
一、适用范围
本规范适用于《医疗器械分类目录》中第二类医用X射线诊断设备(以下简称X射线机)。产品类代号为6830-2。
二、技术审查要点
(一)产品名称要求
X射线诊断设备的命名应采用《医疗器械分类目录》或国家标准、行业标准上的通用名称,或以产品结构和应用范围为依据,例如移动式C形臂X射线机,全景牙科X射线机,不能仅用“X射线机”通称。
X射线机也可称X射线系统、X射线装置。不得使用“X光机”、“X摄影机”、“X线机”等不规范的名称。
(二)产品的结构和组成
1.产品的结构和组成
该产品主要由X射线发生装置、X射线成像装置和附属设备三大部分构成。
X射线发生装置:主要包括X射线源组件、高压发生器等;
X射线成像装置:主要包括X射线电视系统、荧光屏、胶片暗匣、电影摄影机、录像装置、CCD数字摄像系统、CR成像板、DR平板探测器、数字图像系统等;
附属设备:主要包括机械设备如检查床、诊断床、摄影床等,各种支撑、悬吊、保持装置,滤线栅等。
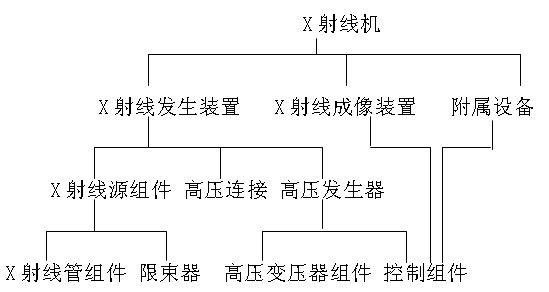
图1 X射线机组成
2.产品的分类
该产品由于结构、功能、特性不同,分类较为复杂,常用分类如下:
2.1按结构分类:
携带式、移动式、固定式。
2.2按使用功能分类:
通用型医用诊断X射线机、透视专用X射线机、摄影专用X射线机、床旁摄影X射线机、车载X射线机、牙科专用(单片)X射线机、乳腺X射线机、胃肠X射线机、X射线骨密度仪等。
2.3按X射线发生装置特性分类:
非工频X射线机/工频(50/60Hz)X射线机、旋转阳极/固定阳极/组合式机头X射线机。
2.4按采集图像方式分类:
胶片感光、荧光屏、电视链(影像增强器、CCD摄像机、显示器及其图像处理系统)、CR、DR。
3.典型产品外型结构示意图
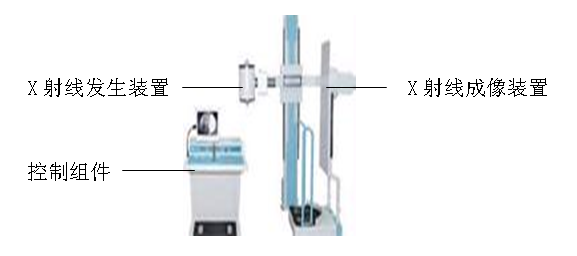
图2 固定式X射线机
(三)产品工作原理/作用机理
1.X射线基本特性
X射线特性主要包括穿透性、荧光性和电离性,其中穿透性、荧光性主要应用于X射线诊断。穿透性是指X射线穿过一定厚度物质的能力。X射线穿过物质的能力与X射线的波长有关,即波长越短,光子能量越大,穿过物质的能力越强。但在波长一定的条件下,X射线穿透性就完全取决于物质本身的结构和性质。一般高原子序数,且结构紧密、密度大的物质,X射线穿透性差,所以从X射线穿透物质后强度变化就反映物质内部密度差异,这正是X射线成像的基础。荧光性是指X射线照射某些物质如磷、硫化锌、镉、钨酸钡等后,可以辐射出可见光,在X射线诊断工作中利用这种荧光作用制成荧光屏,用于X射线透视诊断。
2.X射线机工作原理
高压发生器产生高电压作用于X射线管组件两极,使X射线源组件阴极灯丝(钨丝)上的电子在真空管内高速运动,撞击高密度阳极靶,产生X射线。
临床使用X射线透视和摄影时,X射线发生装置发出X射线穿透人体骨骼、肌肉等密度不同的组织,将透过人体组织载有影像信息的X射线通过荧光屏或胶片、探测器等影像接收装置,转换成可见的密度不同的人体组织的影像,或经过对透射的X射线进行一定处理进行成像,最后根据影像进行临床诊断。
3.X射线机作用机理
因该产品为非直接治疗类医疗器械,故本规范不包含产品作用机理的内容。
(四)注册单元划分的原则和实例
注册单元划分应根据设备的预期用途、性能指标、技术结构进行综合判定。
1.不同预期用途的X射线机,不能作为同一注册单元。
例如,牙科X射线机和乳腺X射线机不能作为同一注册单元;专用透视X射线机和专用摄影X射线机不能作为同一注册单元;车载X射线机和乳腺X射线机不能作为同一注册单元。
2.预期用途相同,性能指标相近,但技术结构有较大差异的X射线机不能作为同一注册单元。
例如,高压发生器结构不一致的(非工频、工频等)、X射线管结构不一致的(固定阳极、旋转阳极、组合式机头等)、关键成像器件工作原理不同的(摄像管、影像增强器、CCD、平板探测器等)、关键组件位置关系不同的(床上管、床下管等)、外观样式差异较大的(微型、C形臂、车载等)、可移动性差异较大的(固定式、移动式、携带式等)、设备电源部分结构有较大区别的(电气安全类型为I类的设备、电气安全类型为II类的设备等)、适用电源条件不同的(a.c.220V、a.c.380V等)不能作为同一注册单元。成像部分有线连接和无线连接可以作为同一注册单元。
3.性能指标有较大差异的,并且因性能指标差异而导致产品结构和功能有较大差异的X射线机,不能作为同一注册单元。
例如,设备的最高标称电功率有较大差异导致产品结构不同的X射线机不能作为同一注册单元。
4.在预期用途相同,性能指标相近,技术结构相同的前提下,一台高压发生装置可以选配不同的床台和成像装置组合成多种配置作为同一注册单元,而任何床台或成像装置不能选配不同的高压发生装置构成一个注册单元。
例如,一台胃肠诊断床不能选配不同的高压发生装置作为同一注册单元。
(五)产品适用的相关标准
根据产品自身特点适用表1中相关标准:
表1 相关产品标准
上述标准包括了产品技术要求中经常涉及到的部件标准和方法标准。有的企业还会根据产品的特点引用一些行业外的标准和一些较为特殊的标准。
产品适用及引用标准的审查可以分两步来进行。首先对引用标准的齐全性和适宜性进行审查,也就是在编写产品技术要求时与产品相关的国家、行业标准是否进行了引用,以及引用是否准确。可以通过对“符合性声明”中声明符合的相关标准是否齐全、适宜来进行审查。此时,应注意标准编号、标准名称是否完整规范,年代号是否有效。其次对引用标准的采纳情况进行审查。即所引用的标准中的条款要求,是否在产品技术要求中进行了实质性的条款引用。
上述标准如有新版发布实施,应执行最新版本。
(六)产品的适用范围/预期用途、禁忌症
该产品产品通过对人体透视和摄影用于医学影像诊断。根据申报资料,审查其预期用途,界定适用范围(如有具体作用部位,应在适用范围中明确)。
禁忌症:暂未发现。
(七)产品的主要风险及研究要求
该产品的风险管理报告应符合YY/T 0316-2008 《医疗器械 风险管理对医疗器械的应用》的有关要求,审查要点包括:
1.产品定性定量分析应依据YY/T 0316-2008中附录A。
2.危害分析应依据YY/T 0316-2008中附录D。
3.风险可接收准则,降低风险的措施及采取措施后风险的可接收程度,是否有新的风险产生。
以下依据YY/T 0316-2008中附录D从八个方面列举了X射线机产品的危害分析。
表2 X射线机危害分析
(八)产品技术要求应包括的主要性能指标
X射线机应符合行业标准YY/T 0106-2008 《医用诊断X射线机通用技术条件》的要求,有专用标准的应符合专业标准的要求。X射线机的关键部件,如X射线管组件、限束器、高压发生器、成像器件等的型号应进行限定。X射线机的应用部分,如诊断床床面板等,建议在研究资料中考虑其生物相容性要求。
1.电功率
1.1最大输出电功率;
1.2标称电功率。
2.加载因素及控制
2.1X射线管电压
2.2X射线管电流
2.3加载时间
2.4电流时间积
2.5防过载
2.6点片摄影准备时间
2.7自动照射量控制(数字化摄影系统考虑)
2.8X射线野与影像接收面之间的对应关系(数字化摄影系统考虑)
3.成像性能
3.1间接摄影和间接透视成像性能
3.1.1规定条件下系统的线对分辨率
3.1.2规定条件下系统的低对比度分辨率
3.1.3影像接收器入射面空气比释动能和(或)空气比释动能率
3.1.4X射线机的入射空气比释动能和(或)空气比释动能率
3.1.5备有空气比释动能面积乘积指示器的设备,应规定其指示的空气比释动能面积乘积值的总准确度
3.2 X射线影像增强器电视系统成像性能
3.2.1有用入射野尺寸
3.2.2影像失真
3.2.3对比度范围
3.2.4图像灰度鉴别等级
3.2.5线对分辨率
3.2.6低对比度分辨率
3.2.7入射空气比释动能率
3.2.8自动透视情况下的图像亮度稳定度
3.2.9图像响应时间
3.3荧光屏透视成像性能(胃肠X射线机考虑)
3.3.1荧光屏的有效尺寸
3.3.2线对分辨率
3.3.3入射空气比释动能率
3.4数字化医用X射线摄影系统成像性能
3.4.1空间分辨率
3.4.2低对比度分辨率
3.4.3影像均匀性
3.4.4有效成像区域
3.4.5残影
3.4.6伪影
3.5乳腺X射线机成像性能
3.5.1总滤过
3.5.2自动照射量控制(AEC)系统
3.5.3乳房托板的上表面与影像接受器平面之间的材料衰减率
3.5.4伪影
3.5.5活动防散射滤线栅影的淡化
3.5.6高对比度分辨率
3.6口腔X射线机成像性能
3.6.1X射线束的限制和校准
3.6.2焦点至皮肤距离
3.6.3线对分辨率
3.6.4低对比度分辨率
3.6.5带增感屏的X射线胶片暗匣
3.6.6图像均匀性
3.7微型医用诊断X射线机成像性能
3.7.1显示屏亮度
3.7.2空间分辨率
3.7.3灰度等级
4. 机械装置性能
4.1机械运动范围
4.1.1如适用,附属设备应规定转动角度范围和纵向、横向、垂直方向运动范围及其偏差值等。
4.1.2C 形臂X射线机应考虑:C 形臂的滑转、C 形臂的旋转、C 形臂的移动、水平摆动、C 形臂的焦点-影像接收器距离、C 形臂的弧深度和C 形臂的开口距离。
4.2长度指示值
4.3角度指示值
4.4制动力
4.5启动力
4.6承重
4.7噪声
4.8移动性能(移动式X射线机考虑)
4.9压迫装置(乳腺X射线机考虑)
4.9.1压迫运动的控制
4.9.2运动范围
4.9.3压迫板
4.9.4压力
4.9.5机械防护
5.软件功能
5.1网络通信
5.2信息管理
5.3成像时间
5.4预览时间
5.5其他
6.高压电缆插头、插座
7. 遥控装置
8. 车载X射线机还应考虑以下要求
8.1运载车辆
8.2输入电源
8.2.1标记
8.2.2输入电源的连接
8.3安装稳定性
8.4保护接地
9. 移动式摄影X射线机还应考虑以下要求
9.1内部电源容量
9.2移用状态外形尺寸
10. 微型医用诊断X射线机还应考虑以下要求
10.1有效视野尺寸
10.2应配有限束器
10.3焦屏距及焦皮距
10.4附加防护屏
10.5加载条件下的泄漏辐射
11.外观
12. 电气安全
应符合GB 9706.1-2007《医用电气设备 第一部分:安全通用要求》及相关安全专用标准的要求。
13.环境试验
应符合YY/T 0291-2007《医用X射线设备环境要求及试验方法》标准的要求。
14.电磁兼容
应符合YY0505-2012《医用电气设备 第1-2部分:安全通用要求 并列标准:电磁兼容要求和试验》标准的要求。
(九)同一注册单元内注册检验代表产品确定原则和实例
典型产品应是同一注册单元内能够代表本单元内其他产品安全性和有效性的产品。
检测样机的选取应考虑产品功能、性能、预期用途、安全指标、主要部件、结构及其组合方式等,具体原则如下:
1.对功能、性能、预期用途、安全指标、主要部件、结构及其组合方式不同的设备应选取不同的检测样机;
2.对产品性能不同,结构及其组合方式相同的设备,应选取不同的检测样机;
3.对主要部件组合方式不同的设备应选取不同的检测样机;
4.对产品主要部件不同的设备应选取不同的检测样机,例如:高压发生器、影像系统、X射线管、患者支撑装置等;
5.对电源部分结构有较大区别的,应选取不同的检测样机;
6.容量不同的产品应选取最大容量的样机,多配置的产品应选择包括各种配置的典型产品进行检测;
7.成像部分有线连接方式和无线连接方式都应进行检测。
(十)产品生产制造相关要求
应明确产品生产工艺过程,可采用流程图的形式,并说明其过程控制点,且应结合产品实际生产过程细化产品生产工艺介绍,应能体现出外协加工部分(如有)、半成品加工过程,工艺流程图中应明示关键工序、特殊过程(如有)、过程控制点、各生产检验工序对环境的要求、使用的相关设备及对设备精度的要求等相关信息。
应详细介绍研制场地、生产场地情况,并应结合前面介绍的产品加工工艺,以及工序和工位的划分、预计产量、生产线划分等实际需求细化研发、生产、检验、库房场地面积、环境控制等相关情况说明。有多个研制、生产场地,应介绍每个研制、生产场地的实际情况。
(十一)产品的临床评价细化要求
X射线机的临床评价应符合《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)和《医疗器械临床评价技术指导原则》(国家食品药品监督管理总局2015年通告第14号)的要求。
X射线机包含在国家食品药品监督管理总局2014年发布的第12号《关于发布免于进行临床试验的第二类医疗器械目录的通告》(以下简称《目录》)中。所以根据《医疗器械临床评价技术指导原则》(以下简称《原则》)的要求,注册申请人需提交申报产品相关信息与《目录》所述内容的对比资料和申报产品与已获准境内注册的《目录》中医疗器械的对比说明。具体需提交的临床评价资料要求如下:
1.提交申报产品相关信息与《目录》所述内容的对比资料;
2.提交申报产品与《目录》中已获准境内注册医疗器械的对比说明,对比说明应当包括《申报产品与目录中已获准境内注册医疗器械对比表》(见《原则》附件1)和相应支持性资料。
提交的上述资料应能证明申报产品与《目录》所述的产品具有等同性。若无法证明申报产品与《目录》产品具有等同性,则应按照《原则》其他要求开展相应临床评价工作。
(十二)产品的不良事件历史记录
暂未见相关报道。
(十三)产品说明书和标签要求
产品说明书、标签应当符合《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局令第6号和相关标准的要求。
标签和包装标识应符合YY/T 1099-2007《医用X射线设备包装、运输和贮存》行业标准的要求。
(十四)研究要求
根据所申报的产品,提供适用的研究资料。
1.产品性能研究
应当提供产品性能研究资料以及产品技术要求的研究和编制说明,包括功能性、安全性指标(如电气安全与电磁兼容、辐射安全)以及与质量控制相关的其他指标的确定依据,所采用的标准或方法、采用的原因及理论基础。
2.生物相容性评价研究
应对成品中与患者和使用者直接或间接接触的材料的生物相容性进行评价。
生物相容性评价研究资料应当包括:生物相容性评价的依据和方法;产品所用材料的描述及与人体接触的性质;实施或豁免生物学试验的理由和论证;对于现有数据或试验结果的评价。
3.灭菌和消毒工艺研究
终端用户消毒:如适用,应明确推荐的消毒工艺(方法和参数)以及所推荐消毒方法确定的依据
4.产品有效期和包装研究
有效期的确定:如适用,应当提供产品有效期的验证报告。
包装及包装完整性:在宣称的有效期内以及运输储存条件下,保持包装完整性的依据。
5.软件研究
含有软件的产品,应当提供一份单独的医疗器械软件描述文档,内容包括基本信息、实现过程和核心算法,详尽程度取决于软件的安全性级别和复杂程度。同时,应出具关于软件版本命名规则的声明,并明确软件版本的全部字段及字段含义,确定软件的完整版本和发行所用的标识版本。
6.其他资料
证明产品安全性、有效性的其他研究资料。
(十五)出厂检测要求
X射线诊断设备出厂检验应包括外观、性能要求和安全要求三部分。
性能要求至少应包括以下内容:最大X射线管电压、管电流、加载时间和电流时间积,及其调节范围和误差;机械运动范围、转动部位角度(如有)、制动装置的制动力(如有)以及其他重要的机械性能;分辨率、功能、外观、标志的要求。
安全要求应包括:漏电流、电介质强度、保护接地阻抗(如有)。
三、审查关注点
审查中需重点关注以下几个方面:
(一) 产品电气安全性能和主要技术性能指标是否执行了国家和行业的强制性标准,是否引用了适用的推荐性标准。
(二)说明书中必须告知用户的信息是否符合6号令及国家标准、行业标准等的要求,信息是否全面完整。
(三) 产品的主要风险是否考虑全面,并通过风险控制措施及其措施的验证确保使产品的安全性在合理可接受的程度之内。
(四) 产品的预期用途是否明确。
(五) 产品技术要求及综述报告中应对关键部件的型号进行限定。关键部件主要包括球管、高压发生器等。
《医用X射线诊断设备产品技术审评规范》编制说明
一、审评规范起草目的和背景
本规范旨在指导和规范X射线诊断设备的技术审评工作,帮助审评人员理解和掌握该类产品原理、结构、性能、预期用途等内容,把握技术审评工作基本要求和尺度,对产品安全性、有效性作出系统评价。
由于该类设备仍在不断发展,审查员仍需从风险分析的角度认真确认申报产品的预期用途与风险管理是否相当;审查员仍需密切关注相关法规、标准及红外线治疗设备技术的最新进展,关注审评产品实际结构组成、功能、预期用途等方面的个性特征,以保证产品审评符合现行法规安全、有效的要求。
二、审评规范编写的依据
(一)《医疗器械监督管理条例》(国务院令第650号)
(二)《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)
(三)《医疗器械说明书和标签管理规定》(国家食品药品监督管理总局令第6号)
(四)《关于发布医疗器械产品技术要求编写指导原则的通告》 (国家食品药品监督管理总局通告2014年第9号)
(五)关于印发《境内第二类医疗器械注册审批操作规范》的通知(食药监械管〔2014〕209号)
(六)《关于发布免于进行临床试验的第二类医疗器械目录的通告》 (国家食品药品监督管理总局通告2014年第12号)
(七)《医疗器械临床评价技术指导原则》(国家食品药品监督管理总局通告2015年第14号)
(八)《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(国家食品药品监督管理总局公告2014年第43号)
(九)国家食品药品监督管理部门发布的其他规范性文件
三、审评规范中重点内容说明
(一)产品名称要求中对产品的命名原则做出了规定。
(二)X射线机的组成参考IEC 60788:1984《医用放射学 术语》。
(三)在产品的工作原理/作用机理中,主要介绍了X射线的特性以及设备的工作原理。
(四)因该类产品因预期用途的不同,结构组成及性能指标差异较大,所以本规范给出了划分同一注册单元的基本要求。
(五)产品的主要性能指标中给出了产品需要考虑的各个方面,主要是参照相关的国家标准、行业标准。
(六)产品的主要风险中,参照YY/T0316中附录D,逐项考虑产品自身以及与配套附件使用时可能产生的危害以及危害发生的原因分析。
(七)不良事件历史记录的确定主要来自国家及北京市不良反应中心的信息,也征询了相关领域的临床专家,尚未发现不良事件。
四、审评规范编写人员和联系方式
本审评规范的编写成员由北京市食品药品监督管理局医疗器械产品注册技术审评人员、行政审批人员及有关方面的专家共同组成,以充分利用各方面的信息和资源,综合考虑规范中各个方面的内容,尽量保证规范正确、全面、实用。
联系方式:010-87559566。
五、关于本版规范的修订说明
本次修订主要涉及以下内容,具体详见表1规范修订前后对照表及修订说明:
(一)根据国家食品药品监督管理总局对注册技术审查指导原则编写格式的最新要求调整了排版、章节顺序和章节名称,新增了产品生产制造相关要求;
(二)明确了电磁兼容适用标准,并在安全要求中明确提出了电磁兼容符合性要求;
(三)根据最新发布的《医疗器械注册管理办法》更新了规范中适用的相关法规,以及审查关注点中提及的申报资料名称;
表1规范修订前后对照表及修订说明

评论区