原文:https://www.cmde.org.cn/splt/ltwz/lttwyq/20220929134325153.html
发布时间:2022-09-29
版权归属原文(原创 2022-09-29 CMDE 中国器审)
感染性疾病是由病原微生物(细菌、病毒、真菌、寄生虫等)引起的疾病的统称。据统计感染性疾病死因占全部死因的25%以上,是当今世界严重威胁人类健康的重大疾病。
长期以来感染性疾病的诊断和疗效监测一直依靠形态学、免疫学、分子生物学以及病原体分离培养等方法,这些方法各有优缺点,在感染性疾病的辅助诊断中发挥着重要作用。
近年来新兴的病原体宏基因组高通量测序(metagenomic next-generation sequencing,mNGS)技术,是指采用高通量测序技术对特定临床样本中所有核酸进行测序,并通过生物信息学分析判断样本中是否存在病原体的检测方法。与传统基于分离培养的病原体检测技术相比,该技术从理论上讲能够无偏倚的检测各类微生物(如:病毒、细菌、真菌、寄生虫等),包括难以培养的病原体以及新发病原体。mNGS技术是一个开放的分析和诊断系统,对于mNGS技术所检测的病原体数量未有明确规定,根据不完全统计,开展相关检测服务的机构已纳入的病原体有近万种,包括细菌、病毒、真菌和寄生虫等,为疑难危重症及罕见病原体感染的诊断提供了有效的技术手段。在特定的临床应用场景下,具有临床意义。
针对mNGS的临床应用,目前已有多个临床专家共识。结合该技术的特点,我中心对相关产品的临床应用、设计开发、验证确认等方面进行了专题研究,现将当前的几点考虑总结如下。
一、关于产品预期临床使用场景
基于mNGS技术的产品与常规的病原体检测产品相比,具有检测过程较为复杂、易受到人源基因的干扰、检测时间较长、结果解读专业要求高、检测成本高等特点,一般用于传统检验方法未能给出明确病原学结果从而影响患者准确诊疗的感染性疾病、新发突发传染病、危急重症或排除其他发热疾病。推荐临床通过拟诊先行传统微生物检验及常规分子生物学产品检测常见病原体,不盲目使用mNGS技术。在必要或紧急情况下,如危急重症、群体性感染事件等,可考虑与常规方法同步进行检测。对常规微生物学检查容易明确的病原体不建议进行mNGS检测。从临床角度,mNGS结果不能单独作为病原学确诊或排除的证据。适用场景举例如下:
(一)患者表现为发热或发热症候群,病因未明确(符合不明原因发热定义),考虑感染或不除外感染,但规范性经验抗感染治疗无效,在应用常规技术检测的基础上,开展mNGS产品检测。
(二)各种原因导致患者急危重症表现,不除外感染所致,或考虑继发或并发危及生命的严重感染,在常规检测的基础上,开展mNGS产品检测。
(三)免疫受损患者疑似继发感染,常规病原学检查未能明确致病原或/和规范性经验抗感染治疗无效,建议进一步完善常规病原学检测的同时,或在其基础上,开展mNGS产品检测。
(四)疑似局部感染,病原学诊断未明确、不及时处理则后果严重时,在常规检测的基础上,开展mNGS产品检测。
(五)高度疑似感染性疾病,但病原学诊断未明确且常规抗感染治疗无效,建议进一步完善常规病原学检测、处理原发感染灶,调整经验抗微生物治疗方案的同时开展mNGS检测。
(六)慢性感染,或慢性疾病不除外感染,尤其是二者临床表现相似、难以鉴别时,病情严重或抗感染治疗疗效不佳需要明确病因,建议在完善常规检测、调整经验治疗的同时开展mNGS产品检测。
(七)其他患者疑似特殊病原体感染或从相关流行病学角度考虑需要进行mNGS产品检测。
二、关于产品的检测样本及适应证
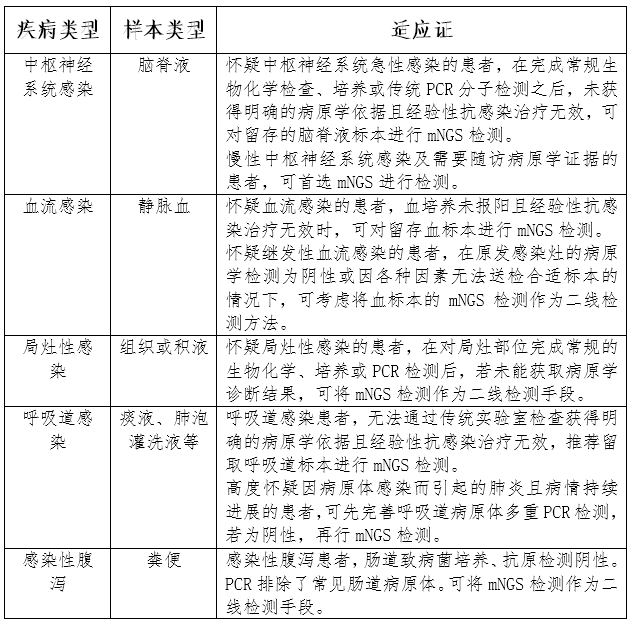
mNGS产品在目前的临床应用研究中涉及多种适应证,如:中枢神经系统感染、血流感染、局灶性感染、呼吸道感染、感染性腹泻等,对于具有相关临床症状的病例,应在按照现有诊疗流程进行标准化诊疗的基础上开展检测。针对患者感染部位不同,采集的样本类型也不同,产品适用的样本类型主要包括:静脉血、脑脊液、痰液、肺泡灌洗液、胸腔积液、腹水、组织、局灶穿刺物、粪便等多种类型。对于样本的采集,应注意以下两个方面,一是,对于无菌体液,如静脉血、脑脊液、胸腔积液、腹水等,需按照严格的无菌操作采集样本,采集的样本须置于无菌容器内;二是,对于有菌部位的样本,如痰液、肺泡灌洗液、咽拭子等,应标明样本的采集部位,在样本采集过程中应尽量避免引入该部位的正常菌群,以免干扰后续检测结果。采集的样本应尽量选取感染部位的体液或组织,可提高检测结果的可信度。若感染部位的样本采集难度较大,可选择外周血液样本,但有可能会降低检测结果的准确性。产品适用的样本类型推荐优先选择无菌采集的样本。关于不同适应证适用的样本类型举例见表1。
表1.产品适应证与适用的样本类型举例
三、关于产品检测病原体种类范围
mNGS产品检测原理为对临床样本中存在的病原体核酸进行无偏倚的检测,从产品检测的技术角度考虑,除新发病原体外,产品的检测范围不应局限为某一种或某几种常见病原微生物,应为产品适应证、适用样本中所有可报告的病原微生物。产品所检测的病原微生物受几个方面的影响,一是产品配套使用的参考数据库及生信分析过程涵盖的病原体种类,如数据库中未涵盖某种病原体基因组参考序列,则该类病原体不在该产品的检测范围之内;二是检测样本类型、核酸提取等会直接影响产品病原体的检测种类,不同的样本类型可能检出的病原体会存在差别,如脑脊液样本检出的病原体主要以中枢神经系统感染的病原体为主,而粪便样本检出病原体主要为消化系统感染的病原体。不同的核酸提取方式对病原体的检出种类也会产生影响,如核酸提取过程未考虑破壁,则产品可能不适用于具有厚细胞壁的病原体检测;三是产品检测的目标物是否包括不同类型的核酸靶标,如产品检测的靶标仅为DNA,则RNA病毒不在该产品的检测范围之内。相关产品的申请人应依据产品设计、适用的样本类型、适应证等多个方面综合考虑产品预期用途,确定合理的病原体检测范围。
四、关于产品配套使用的数据库
mNGS产品检测结果,除了产生可用于比对的微生物短片段序列外,还存在大量人源、环境微生物、试剂含有的微生物等背景核酸序列,必须依靠生物信息学手段对其进行筛选、过滤、比对,最终给出微生物物种注释。结果分析过程中,数据库的使用是必需的,而且是影响mNGS产品检测结果准确性的重要因素。目前相关产品在选择配套使用的数据库时,一般会存在两种情况,一种为直接选择公共数据库,如:NCBI nr/nt database、NCBI RefSeq database等;另一种为自建数据库,对公开数据库中基因组序列进行挑选、整理、分类,然后通过程序软件将收集到的基因组序列整理成适用于本产品的微生物及人源序列比对数据库。针对成熟的产品,建议根据产品特点及临床需要,使用临床应用级的自建数据库。在数据库的构建、使用和管理方面应注意以下问题:
(一)需要考虑数据库的全面性以及纳入物种在分类学上的代表性,对于同一种微生物,往往存在具有遗传差异的不同亚型或株,所以在选择基因组时,应考虑到微生物的遗传多样性,尽可能选取具有高度代表性的不同亚型或株的高质量基因组。
(二)无论所选择的参考基因组的来源如何,申请人需要考虑其注释的准确性及序列的完整性,防止注释错误、命名错误或者代表性不足临床相关微生物列入库。
(三)申请人应在有必要的基础上,对纳入库中的微生物的潜在的临床意义进行注释,让结果解读人员对检测的微生物有基本的认识和判断。
(四)由于病原体在自然状态下是不断发生进化变异的,致病性也是动态变化的,所以需要及时(或定期)对参考数据库中的基因组信息及临床致病证据进行更新。
(五)当数据库发生可能影响病原体判读结果的更新后,应对更新后的数据库进行验证与确认。
(六)应构建全面的人源基因序列数据库,并评估最新版国际人类参考基因组和用于构建人源基因序列数据库所选择的参考基因组差异,进而评价人源基因序列数据库的代表性,人源基因序列数据库用于在生信分析过程中过滤人源基因数据。
(七)mNGS检测产品检测过程中一些样本中会存在背景菌序列、环境微生物及实验室残留微生物,这些基因序列可造成测序污染,导致假阳性结果产生;另外,一些样本(例如呼吸道样本)会存在定植微生物,因此,针对产品需要构建检测背景库用于过滤污染序列、区分背景病原体和致病性病原体。
五、关于测序数据要求
人体不同的样本类型单位体积含有的细胞数量有巨大的差异,最终的测序数据由微生物序列和人源基因组序列组成,不同的人源细胞含量、病原微生物感染的类型和病原体含量的高低都会影响测序数据中目标微生物序列占比,如组织样本的人源细胞含量比较高,测序所得的序列数据中相应微生物的占比可能较少,因此,mNGS产品在不同的样本类型中,产品分析灵敏度会存在差异。该类产品可通过增加测序数据量来提高待检出的微生物数据量,或通过富集微生物含量以提升微生物序列的占比,从而提高微生物的检出率。一般而言,在一定范围内随着测序数据量的增加,产品的灵敏度会有所提升。因此,为了保证产品具有满足临床要求的灵敏度,针对某一样本类型,应保证一定的测序数据量。产品在设计上,一般分为去除宿主人源基因与未去除宿主人源基因两种设计,去除宿主人源基因后,产品产生的相应数据量会大大减少。在缺乏有效的人源宿主去除步骤的情况下,单个样本检测所需的数据量应充分评估并设立合理的指标要求。
测序模式一般为单端测序和双端测序,双端测序所花费的经济成本及时间均高于单端测序,如产品设计选择单端测序,为确保序列比对的准确性,避免因同源错配导致的序列比对错误,可参考相关专家共识的要求,如测序序列单端读长当前建议不少于50bp。
为了保证数据分析的可靠性,产品检测的下机数据应有一定的质量要求。下机数据经拆分后即得到每个样本的测序数据,需要进行数据质量过滤,包括过滤测序接头、低质量序列、低复杂度序列、重复序列等,将获得的高质量读长序列作为微生物鉴定的输入数据。一般而言,数据应达到以下指标:Q30碱基数量占比>80%、接头污染比例不超过1%、有效序列长度不小于50bp、数据的有效比对率应大于70%等。
六、关于产品阳性判断值的研究
产品阳性判断值的研究,主要是为了区分真阳性、真阴性,以及判断实验过程中污染的微生物等。
基于mNGS技术的产品,阳性判断值应包含度量标准,例如检测结果中能够比对到数据库中的微生物的序列数、对某种微生物的基因组覆盖度等,可通过ROC曲线分析的方法对产品的阳性判断值进行研究。
在阳性判断值研究过程中应注意,胞内菌和厚壁微生物检出率低,因此即使在检测报告中某种/某些胞内菌/厚壁菌检出序列数不高,也要考虑其为致病病原体的可能。
七、关于产品检测结果的报告
用于临床辅助诊断的mNGS报告应包括测序总序列数、检测病原微生物列表、检出病原特异序列数量、检测病原范围、覆盖度、测序深度、检测方法及检测技术说明。需要注意的是,检测结果仅代表临床样本中检出或未检出某微生物的核酸片段,不能明确该物种与感染的关系,即使阴性结果也需结合临床表现及其他检查结果进行综合判断。
对于胞内菌和厚壁微生物的检测,因技术原因存在一定的偏倚,如对于胞内感染菌因释放到体液中含量较少而导致检测敏感性偏低,对具有较厚细胞壁的病原微生物如真菌感染,可能由于核酸提取效率较低,相对检出率低,导致临床检出率和敏感性较低。因此即使在检测结果中某种胞内菌/厚壁菌检出序列数不高,也要考虑其为致病病原体的可能。mNGS信息量大,临床应用过程中,检验机构依据检测结果出具检验报告时,有些情况下不可能在结果中列举出所有检测到的病原体,对于罕见病原体、胞内菌等,可能因检出序列数少、微生物丰度低,在报告中未能列举,如果临床有疑似特殊病原体的感染,应该可以追溯原始数据库进行查询。
八、关于产品验证与确认的考虑
基于mNGS技术的产品,因其预期用途涵盖的病原体的种类非常广,产品验证与临床试验应对检测范围内的病原体进行有充分覆盖度、有充分代表性的性能评价。产品临床试验在入组人群上,应与产品临床适用人群一致。在对比方法选择上,应选择临床参考方法作为对比方法,临床参考方法应综合病原体分离培养、患者的影像学检查结果、基于宿主反应的检测结果等。同时,由mNGS获得致病病原体后,临床上会针对病原体进行精准治疗,治疗后患者的临床表现和治疗效果的随访结果也可以作为临床试验对比方法的证据。
临床试验过程中,应关注试验体外诊断试剂对一些对于胞内感染菌、具有较厚细胞壁的病原微生物等的临床性能研究。
参考文献:
1.宏基因组分析和诊断技术在急危重症感染应用的专家共识[J].中华急诊医学杂志,2019(02):151-155.
2.宏基因组学测序技术在中重症感染中的临床应用专家共识(第一版)[J].中华危重病急救医学,2020,32(05):531-536.
3.《中华传染病杂志》编辑委员会.中国宏基因组学第二代测序技术检测感染病原体的临床应用专家共识[J].中华传染病杂志,2020,38(11):681-689.
4.中华医学会检验医学分会.高通量宏基因组测序技术检测病原微生物的临床应用规范化专家共识[J].中华检验医学杂志,2020,43(12):1181-1195.
5.宏基因组高通量测序技术应用于感染性疾病病原检测中国专家共识[J].中华检验医学杂志,2021,44(02):107-120.
6.中华医学会检验医学分会.宏基因组测序病原微生物检测生物信息学分析规范化管理专家共识[J].中华检验医学杂志,2021,44(09):799-807.
7.Charles Y. Chiu and Steven A. Miller Clinical metagenomics Nature Reviews Genetics 2019,20, 341-355.
8.fda. Infectious Disease Next Generation Sequencing Based Diagnostic Devices:Microbial Identification and Detection of Antimicrobial Resistance and Virulence Markers(Draft)

评论区